Cladribina Referencias Menú de navegación4291-63-8BB0420279DB00242567361
Agentes antineoplásicosNucleósidos
tricoleucemiaJanssenJohnson & JohnsonAgencia Europea de Medicamentosesclerosis múltipleMerck KGaAFDA
| Cladribina | ||
|---|---|---|
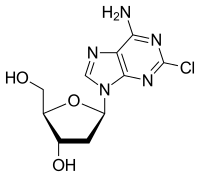 | ||
| Nombre (IUPAC) sistemático | ||
5-(6-amino-2-chloro-purin-9-yl)-2-(hydroxymethyl)oxolan-3-ol | ||
| Identificadores | ||
| Número CAS | 4291-63-8 | |
| Código ATC | L01BB04 | |
| PubChem | 20279 | |
| DrugBank | DB00242 | |
| ChEBI | 567361 | |
| Datos químicos | ||
| Fórmula | C10H12N5ClO3 | |
| Peso mol. | 285.687 g/mol | |
| Farmacocinética | ||
| Vida media | 5.4 horas | |
| Datos clínicos | ||
| Vías de adm. | Oral, IV, SC | |
La cladribina es un fármaco antineoplásico que se usa en el tratamiento de la tricoleucemia.[cita requerida] Es comercializada bajo el nombre comercial Leustatin en forma inyectable por via intravenosa de 10 mg (1mg/mL) por el laboratorio Janssen, del grupo Johnson & Johnson.
El 25 de agosto de 2017, la Agencia Europea de Medicamentos aprobó una formulación oral de cladribina para formas recurrentes de esclerosis múltiple altamente activa. Es comercializada por Merck KGaA de Alemania y sus filiales o agentes en el mundo, bajo el nombre comercial Mavenclad tabletas 10 mg. Mavenclad ya fue aprobado por agencias regulatorias de Canadá, Argentina, Chile, Emiratos Arabes Unidos o Australia, entre otros. Se espera su aprobación por FDA para el año 2019.